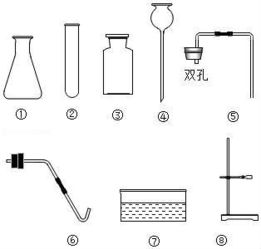
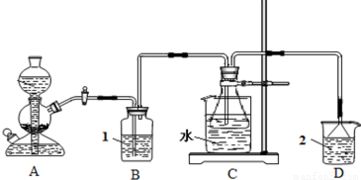
在化学实验室中,利用现有资源进行日用化学产品的设计与制造,是连接基础化学知识与实际应用的重要桥梁。实验室现有氯酸钾(KClO₃)、二氧化锰(MnO₂)、石灰石(主要成分CaCO₃)、稀盐酸(HCl)和稀硫酸(H₂SO₄)等原料,结合常规仪器(如试管、烧杯、集气瓶、导管、酒精灯、铁架台等),我们可以模拟或小规模制备一些贴近生活的化学品。以下是根据这些条件,围绕“日用化学产品制造”这一主题进行的探索性方案。
一、 清洁与消毒类产品原理模拟
1. 氯系消毒剂的制备原理:
氯酸钾在二氧化锰的催化下加热,可以制取氧气(2KClO₃ →(MnO₂, △) 2KCl + 3O₂↑)。虽然直接产品是氧气,但此反应展示了固体催化剂在分解反应中的应用,这是许多化工生产过程(包括某些消毒剂生产中的中间步骤)的缩影。实验室制得的氧气本身也具有支持燃烧和某些氧化消毒的潜力。
2. 酸性清洁剂的原理验证:
石灰石(CaCO₃)与稀盐酸反应,是模拟洁厕剂或除垢剂工作原理的经典实验(CaCO₃ + 2HCl → CaCl₂ + H₂O + CO₂↑)。产生的二氧化碳气体可证明其除垢(去除碳酸钙水垢)效果。此实验直观展示了酸性清洁剂如何通过化学反应溶解碱性污垢。若使用稀硫酸,反应生成微溶的硫酸钙会覆盖在石灰石表面阻碍反应,这恰好可以对比说明不同酸在清洁剂配方中的选择依据。
二、 教学演示与模型构建
利用这些原料和仪器,可以构建一个微型的“化学制造”演示系统:
- 气体发生装置:用石灰石与稀盐酸制取二氧化碳,可用于模拟碳酸饮料中充气过程,或演示灭火原理(二氧化碳不支持燃烧)。
- 催化反应装置:用氯酸钾与二氧化锰制氧,可演示催化作用,并收集氧气用于后续实验(如助燃),模拟工业制氧或氧化剂生产的基本单元。
三、 安全警示与创意延伸
在尝试任何制备时,安全是第一原则:
- 氯酸钾是强氧化剂,加热时必须严格控制温度,避免与可燃物混合,防止爆炸危险。
- 使用酸类时需佩戴防护用具,在通风处操作。
- 所有实验产物均为实验室级别,不可直接作为日用品使用,仅用于原理探究。
创意延伸思考:
尽管原料有限,但通过组合与思考,可以深化对日化产品制造的理解。例如,思考如何将生成的二氧化碳通入澄清石灰水(可另行制备)来制造“云雾”效果(碳酸钙沉淀),这类似于某些舞台效果或教学演示产品的化学原理。二氧化锰作为催化剂,其回收与再利用过程,也模拟了工业生产中对催化剂处理的环保理念。
结论
通过实验室常见的氯酸钾、二氧化锰、石灰石、稀盐酸和稀硫酸,配合基础仪器,我们能够生动地演示和探索多种日用化学产品(如消毒剂、清洁剂、气体产品)背后的核心化学反应与生产原理。这种实践不仅巩固了无机化学知识,更培养了将理论转化为实际应用的创新思维与安全意识,体现了化学服务于日常生活的巨大价值。